Tự động phát
Kết quả ban đầu về thử nghiệm tiêm chủng quy mô lớn vắc xin ngừa Covid-19 của hãng dược AstraZeneca tại Mỹ, được xem là thành công, hiện đang được rà soát lại bởi Ban Giám sát An toàn Dữ liệu, một ủy ban độc lập giám sát thử nghiệm.
Ban giám sát bày tỏ lo ngại rằng AstraZeneca có thể đã dùng “thông tin lỗi thời” từ cuộc thử nghiệm trên, dẫn đến khả năng tạo ra cách nhìn không toàn diện trong dữ liệu về hiệu quả phòng ngừa. Điều này có khả năng ảnh hưởng đến kế hoạch cấp phép sử dụng khẩn cấp loại vắc xin này trong những tuần tới tại Mỹ.
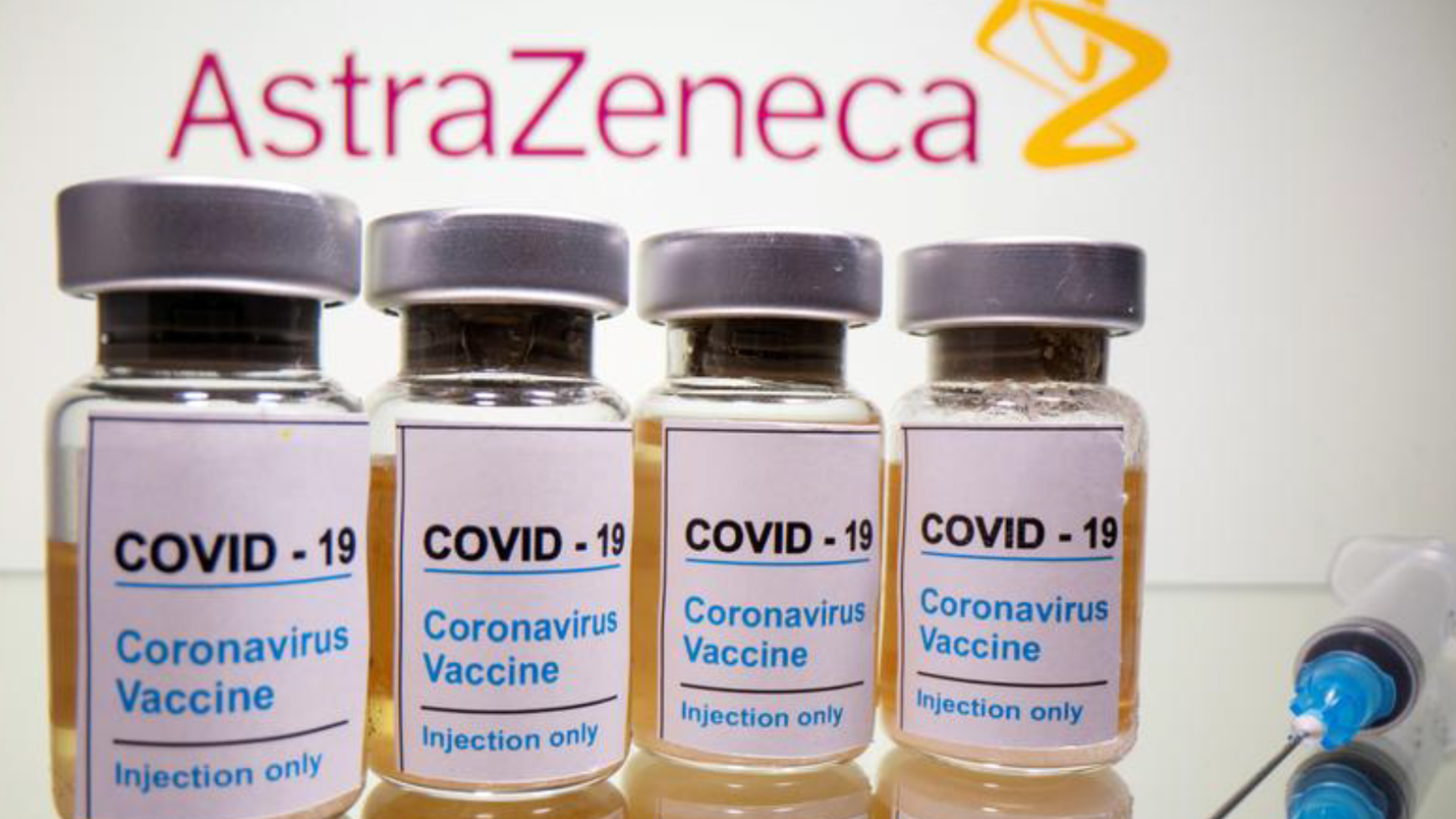
Vắc xin ngừa Covid-19 của hãng dược AstraZeneca trước đó bị tạm ngừng sử dụng do xuất hiện một số tác dụng phụ Reuters |
Theo dữ liệu được công bố hôm 22.3, vắc xin được phát triển bởi Đại học Oxford đạt hiệu quả 79% trong việc ngăn ngừa các triệu chứng của bệnh Covid-19 trong cuộc thử nghiệm lớn trên 32.000 người diễn ra đồng thời ở Mỹ, Chile và Peru. Theo số liệu, vắc xin AstraZeneca cũng đạt 100% hiệu quả đối với các trường hợp bệnh nặng hoặc nghiêm trọng và nhập viện. Ngoài ra, vắc xin này không làm tăng nguy cơ hình thành máu đông.
AstraZeneca hôm 23.3 cho biết các số liệu đã công bố “được dựa trên phân tích dữ liệu tạm thời tính đến ngày 17.2”. Hãng dược cam kết sẽ sớm cung cấp dữ liệu cập nhật nhất về độ hiêu quả.

Thủ tướng Anh Boris Johnson tiêm vắc xin ngừa Covid-19 của AstraZeneca AFP |
Vắc xin ngừa Covid-19 của AstraZeneca đã được cấp phép tiếp thị có điều kiện hoặc sử dụng khẩn cấp ở hơn 70 quốc gia. Sau một thời gian ngắn ngừng sử dụng, nhiều quốc gia châu Âu đã tiếp tục sử dụng loại vắc xin này.
Một số nhà lãnh đạo trên thế giới cũng đã tiêm phòng vắc xin của AstraZeneca để người dân cảm thấy an tâm. Tại Mỹ, Viện Dị ứng và Bệnh truyền nhiễm Quốc gia hiện đang thúc giục công ty xem xét dữ liệu về tính hiệu quả. AstraZeneca đã không trả lời yêu cầu bình luận về vụ việc.





Bình luận (0)